Hallo ich muss eine Auswertung für ein Protokoll vornehmen und habe dabei Schweirigkeiten...
Aufgabe lautet: Versuch Spektralphotometer
1)
Stellen Sie die Wellenlängen der vier deutlich erkennbaren Maxima in den Spektren fest und ordnen Sie diese den beiden Farbstoffen Chl.a und Chl.b zu.
2)
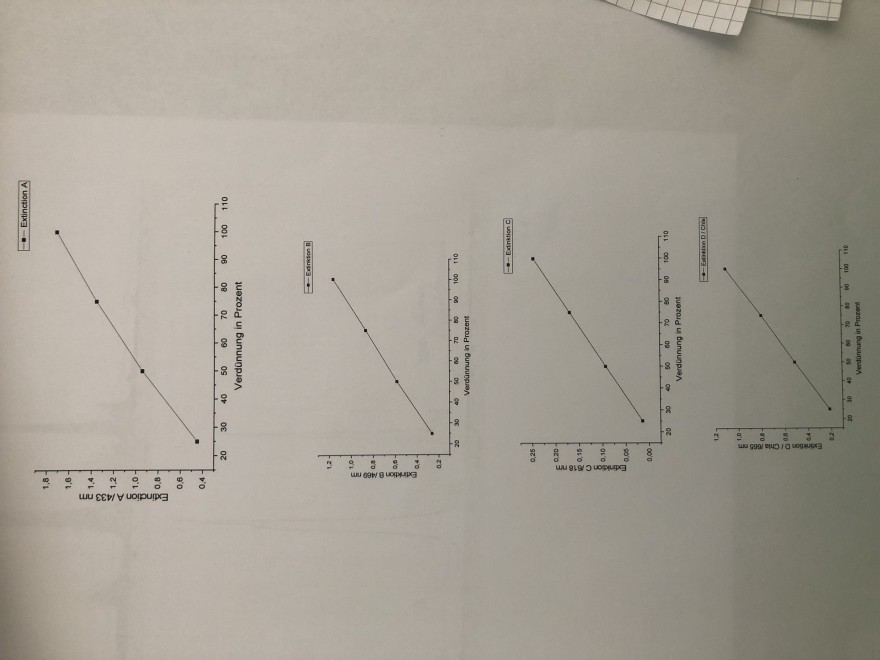
Die Extinktion in allen vier Maxima ist in Abhängigkeit von der Verdünnung grafisch darzustellen und an Hand von Gleichung E = lg I0/I = ε * c * d zu diskutieren.
Problem/Ansatz:
1)
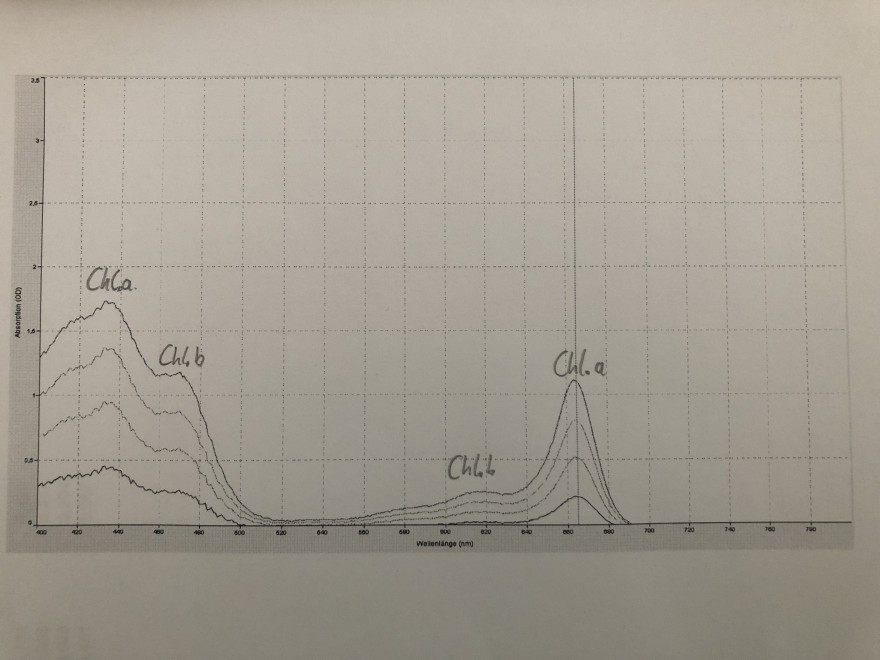
Also ich habe es mit den Literaturen verglichen und dabei soll Chl. a ein Maxima bei 430 und 665 haben und Chl. b bei 453 und 649, diese Wellenlängen kommen annähernd in der Grafik und in den Maxima zum Vorschein... also habe ich diese so beschriftet. Ich bin jedoch verunsichert weil das zweite Maxima bei 453nm eigentlich eine viel höhere Absorbtion haben sollte als bei dem Maxima mit 433nm? Kann mir das Jemand erklären? Ist meine Beschriftung überhaupt so richtig, weil Chl. a und Chl. b sich ja irgendwie in einer Grafik überlagern oder addiert sind?
Zu 2tens habe ich gar keine Vorstellung, würde mich sehr darüber freue,w enn mir das Jemand zeigen könnte...
E = lg I0/I = ε * c * d
lg ist dekadischer Logarithmus
I0 ist einfallende Lichtintensität
I ist hindurchgehende Lichtintensität
ε ist dekadische Extinktionskoeffizient ε = εn/ln = 0,4343 * εn
c ist Konzentration
und d ist glaube der Durchmesser der Küvetten mit d = 10mm
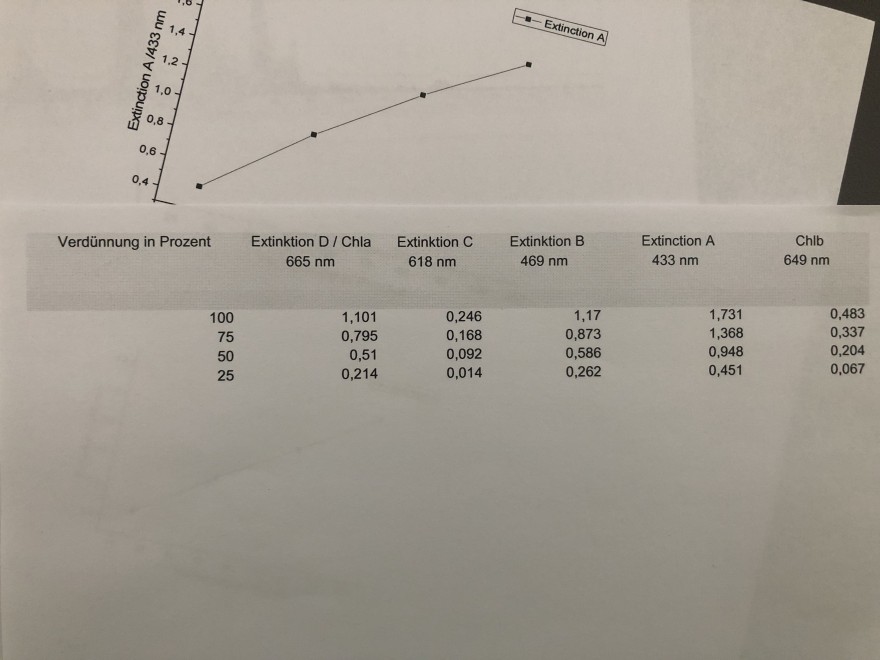
Hier noch die Werte:
Text erkannt:
Verdünnung in Prozent
Extinktion D / Chla
Extinktion \( \mathrm{C} \)
Extinktion B
Extinction A
Chlb \( 665 \mathrm{~nm} \)
\( 618 \mathrm{~nm} \)
\( 469 \mathrm{~nm} \)
\( 433 \mathrm{~nm} \)
\( 649 \mathrm{~nm} \)
\begin{tabular}{rrrr}
100 & 1,101 & 0,246 & 1,17 \\
75 & 0,795 & 0,168 & 0,873 \\
50 & 0,51 & 0,092 & 0,586 \\
25 & 0,214 & 0,014 & 0,262
\end{tabular}
1,731 1,368 0,948 0,451
0,483
0,337
0,204
0,067